Neuralink potrà testare il suo impianto neurale sugli esseri umani
Dopo averlo testato sugli animali (uccidendone oltre 1500 in tre anni), Neuralink ha ottenuto l'autorizzazione a testare il suo impianto neurale sull'uomo.
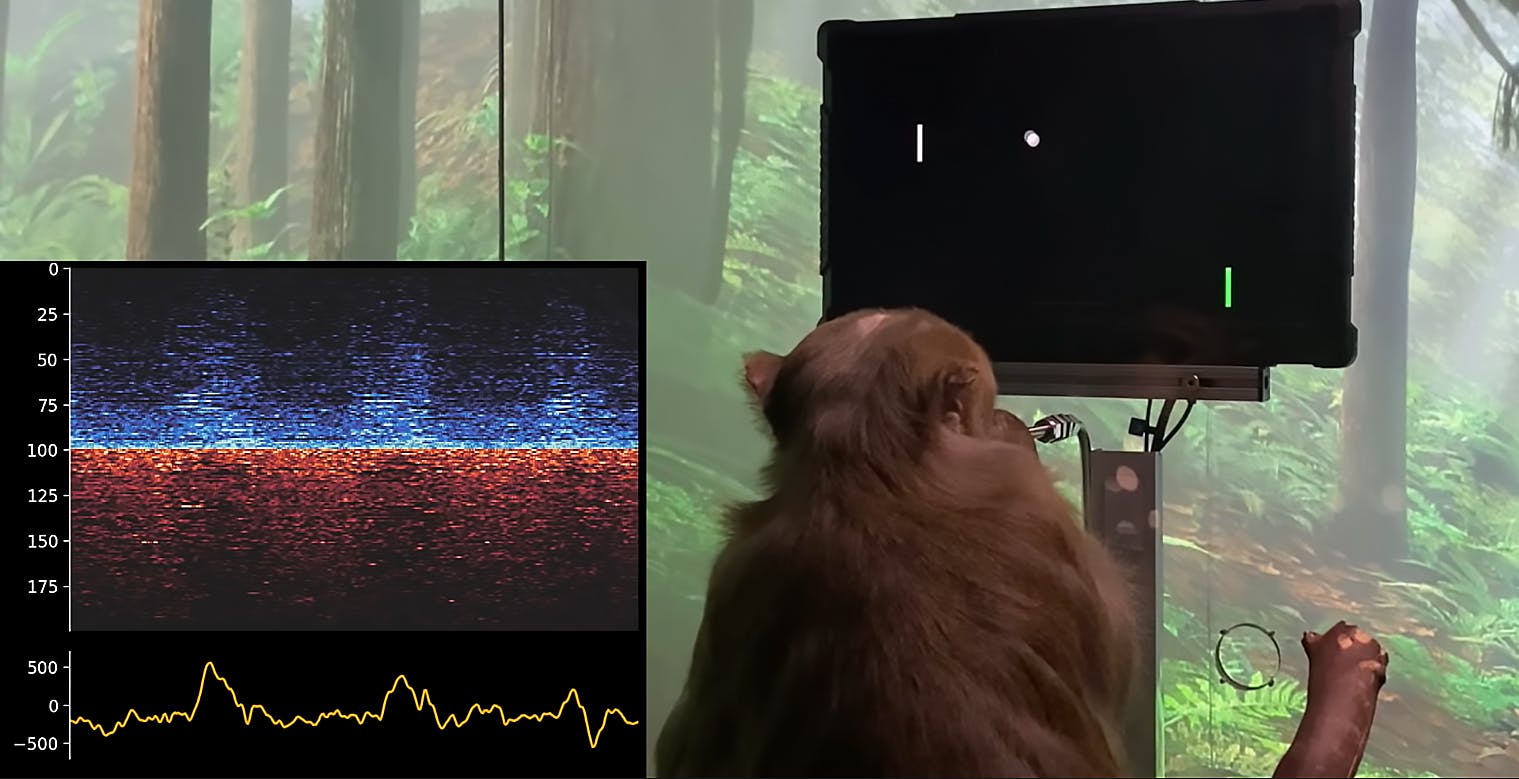
Giovedì la FDA, l’autorità che regolamenta, tra le altre cose, anche l’autorizzazione alla vendita e alla sperimentazione di nuovi farmaci e cure, ha dato il via libera alla richiesta di Neuralink di iniziare i trial della sua interfaccia neurale sugli esseri umani. Il prototipo dell’interfaccia cercello-computer, chiamata Link, era già stato testato su alcuni primati e altri animali.
Fondata nel 2016, Neuralink mira a commercializzare le interfacce cervello-computer in varie applicazioni mediche e terapeutiche, che vanno dal recupero da ictus e lesioni al midollo spinale, al controllo di protesi neurali, fino alla capacità di “riavvolgere i ricordi e salvarli su un computer” — come aveva promesso Elon Musk in un’intervista rilasciata nel 2020.
Le interfacce cervello-computer traducono essenzialmente gli impulsi elettrici analogici del cervello in dati digitali, che possono quindi essere processati da un computer. Poiché queste interfacce devono essere chirurgicamente impiantate nel cervello del paziente, la FDA, che regola tali tecnologie, richiede alle aziende di condurre rigorosi test di sicurezza prima di concedere l’approvazione per l’uso commerciale.
A marzo, la FDA aveva respinto la richiesta di Neuralink di iniziare i trial umani, in parte a causa della notizia che durante i precedenti test, a causa di complicazioni causate proprio dal chip, ma anche per colpa di errori materiali, erano morti oltre 1500 animali. Attualmente è in corso un’indagine dell’Ispettore Generale del Dipartimento dell’Agricoltura degli Stati Uniti per accertare eventuali responsabilità dell’azienda.
Motivando il precedente diniego, la FDA aveva spiegato di aver bisogno di maggiori rassicurazioni. In particolare, l’agenzia temeva che le batterie del chip possano surriscaldarsi, creando danni permanenti al cervello, oppure che i componenti più piccoli dell’impianto possano spostarsi in altre aree del cervello.
