Riparazione delle ferite: la ricerca rivela un nuovo meccanismo protettivo
Un nuovo meccanismo protettivo indipendente dall’infezione entra in funzione in risposta ai segnali di danno nei tessuti feriti
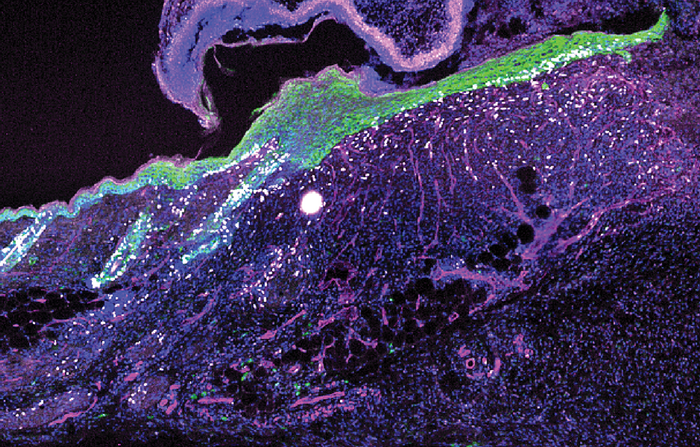
Una nuova ricerca del laboratorio di Elaine Fuchs della Rockefeller, pubblicata su Cell, rivela un meccanismo protettivo alternativo che risponde ai segnali di danno nei tessuti feriti – compresi i bassi livelli di ossigeno dovuti alla rottura dei vasi sanguigni e alla formazione di croste – e non ha bisogno di un’infezione per entrare in funzione. Lo studio è il primo a identificare una via di risposta al danno distinta- ma parallela- a quella classica innescata dagli agenti patogeni. Alla guida della risposta c’è l’interleuchina-24 (IL24), il cui gene è indotto nelle cellule staminali epiteliali della pelle sul bordo della ferita. Una volta scatenata, questa proteina inizia a mobilitare una serie di cellule diverse per avviare il complesso processo di guarigione. “L’IL24 diventa un orchestratore che coordina la riparazione dei tessuti”, spiega Fuchs, responsabile del Robin Chemers Neustein Laboratory of Mammalian Cell Biology and Development. Gli scienziati hanno capito da tempo come il nostro corpo risponde alle minacce indotte dagli agenti patogeni: le cellule riconoscono i batteri o i virus invasori come entità estranee e inducono una serie di meccanismi di difesa con l’aiuto di proteine di segnalazione come gli interferoni di tipo 1. Ma come fa l’organismo a rispondere a un agente patogeno? Se ci tagliamo un dito mentre affettiamo un cetriolo, ad esempio, ce ne accorgiamo immediatamente: c’è sangue e dolore. Tuttavia, il modo in cui il rilevamento di una lesione porta alla guarigione è poco conosciuto a livello molecolare. Mentre gli interferoni di tipo 1 si basano sui fattori di segnalazione STAT1 e STAT2 per regolare la difesa contro gli agenti patogeni, una precedente ricerca del laboratorio Fuchs aveva dimostrato che un fattore di trascrizione simile, noto come STAT3, fa la sua comparsa durante la riparazione delle ferite. Siqi Liu, coautore di entrambi gli studi, ha voluto risalire al percorso di STAT3 fino alle sue origini.
Lo studio
In collaborazione con il laboratorio di Daniel Mucida del Rockefeller, i ricercatori hanno lavorato con topi in assenza di agenti patogeni e hanno scoperto che la cascata di segnalazione dell’IL24 indotta dalla ferita è indipendente dai germi. Ma quali segnali di lesione inducono la cascata? Le ferite spesso si estendono nel derma della pelle, dove si trovano capillari e vasi sanguigni. “Abbiamo scoperto che le cellule staminali epidermiche percepiscono l’ambiente della ferita”, spiega Yun Ha Hur, ricercatore del laboratorio e coautore del lavoro. Quando i vasi sanguigni vengono recisi e si forma una crosta, le cellule staminali epidermiche sul bordo della ferita sono affamate di ossigeno. Questo stato di ipossia (mancanza di ossigeno) è un campanello d’allarme per la salute delle cellule e induce un ciclo di feedback positivo che coinvolge i fattori di trascrizione HIF1a e STAT3 per amplificare la produzione di IL24 sul bordo della ferita. Il risultato è uno sforzo coordinato da parte di diversi tipi di cellule che esprimono il recettore dell’IL24 per riparare la ferita sostituendo le cellule epiteliali danneggiate, guarendo i capillari rotti e generando fibroblasti per le nuove cellule della pelle. In collaborazione con il gruppo di Craig Thompson del Memorial Sloan Kettering Cancer Center, i ricercatori hanno dimostrato di poter regolare l’espressione del gene Il24 modificando i livelli di ossigeno. Una volta individuata l’origine del percorso di riparazione tissutale nelle cellule staminali epidermiche, i ricercatori hanno studiato il processo di riparazione delle ferite in topi geneticamente modificati (con mancata funzionalità di IL24). Senza questa proteina chiave, il processo di guarigione è stato lento e ritardato, richiedendo giorni in più rispetto ai topi normali per ripristinare completamente la pelle. I ricercatori ipotizzano che l’IL24 possa essere coinvolta nella risposta alle lesioni in altri organi del corpo caratterizzati da strati epiteliali, che fungono da guaina protettiva. In studi recenti, è stata rilevata un’elevata attività di IL24 nel tessuto epiteliale polmonare di pazienti affetti da COVID-19 grave e nel tessuto del colon di pazienti affetti da colite ulcerosa, una malattia infiammatoria cronica dell’intestino.
Legati dalla funzione e dall’evoluzione
“I nostri risultati forniscono indicazioni su un’importante via di segnalazione del danno tissutale e della riparazione che è indipendente dalle infezioni“, spiega Fuchs. Un’analisi condotta con il biologo evoluzionista Qian Cong dell’UT Southwestern Medical Center ha rivelato che l’IL24 e i suoi recettori condividono una stretta omologia di sequenza e struttura con la famiglia degli interferoni. Sebbene non lavorino sempre in coordinazione, IL24 e gli interferoni sono evolutivamente correlati e si legano a recettori vicini tra loro sulla superficie delle cellule. I ricercatori sospettano che queste molecole di segnalazione derivino da un percorso molecolare comune che risale al nostro passato. “Pensiamo che centinaia di milioni di anni fa questo antenato possa essersi diviso in due vie: una per la difesa dagli agenti patogeni e l’altra per le lesioni ai tessuti”, spiega Liu. Forse la scissione è avvenuta per far fronte alle crescenti esplosioni di agenti patogeni e lesioni che hanno causato un mare di problemi alla vita sulla Terra.
