Biocarburanti: le microalghe come materia prima per la produzione
Dal Brasile l'idea di usare alcuni elementi delle microalghe per produrre biocarburante
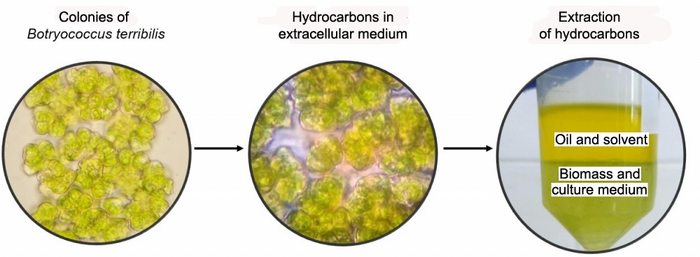
Un gruppo di ricercatori dell’Università Statale di Campinas (UNICAMP) in Brasile ha coltivato microalghe in condizioni controllate in laboratorio per utilizzarne i metaboliti, in particolare i lipidi, con lo scopo principale di produrre biocarburante. Lo studio è riportato in un articolo pubblicato sulla rivista Biomass Conversion and Biorefinery. “È anche possibile estrarre proteine e carboidrati e usarli come cibo, oltre a ottenere prodotti che possono essere usati in cosmetica, come il beta-carotene e altri composti preziosi, tra cui la ficocianina, un pigmento blu naturale“, ha detto Luisa Fernanda Ríos, seconda autrice dell’articolo. Il colore del mare e dei fiumi è spesso dovuto in gran parte alla presenza di microalghe, che possono essere blu, verdi o marroni”. Lo studio ha analizzato la crescita e la produttività della microalga Botryococcus terribilis, confrontando il suo comportamento in sistemi chiusi e aperti. I sistemi chiusi, in cui non c’è scambio d’aria con l’ambiente e le condizioni possono essere strettamente controllate, comprendono i fotobioreattori. I sistemi aperti comprendono i raceway, ovvero stagni o canali artificiali poco profondi in cui circolano le microalghe, l’acqua e le sostanze nutritive e in cui l’aria viene scambiata con l’ambiente. Secondo l’articolo, sono stati estratti e quantificati proteine, carboidrati, lipidi, pigmenti e idrocarburi. Per la prima volta sono stati caratterizzati gli idrocarburi estratti da B. terribilis. Come le piante, le microalghe crescono attraverso la fotosintesi, convertendo l’anidride carbonica atmosferica, l’acqua e la luce solare in energia e generando ossigeno come sottoprodotto. I metaboliti che ne derivano includono proteine, carboidrati e lipidi, oltre a carotenoidi, clorofilla e vitamine in quantità minori. Il petrolio contiene anche microalghe depositate sui fondali marini e nelle profondità del sottosuolo.
Lo stress
Le microalghe sono organismi unicellulari e si riproducono per mitosi: ogni cellula si divide in due cellule figlie identiche, dando luogo a una moltiplicazione esponenziale. “Coltiviamo le microalghe in laboratorio per sfruttare tutti i biocomposti presenti nelle loro cellule. Per farlo dobbiamo ucciderle, ma questo non è un problema perché crescono molto velocemente e sono sempre abbondanti”, ha detto Ríos. Gli oli di B. terribilis sono adatti per la sintesi di biocarburanti, poiché sono composti da idrocarburi a catena lunga e da grandi quantità di acidi grassi saturi e monoinsaturi. Lo studio contribuisce a colmare la lacuna informativa sulla coltivazione, lo stress e la composizione di queste microalghe, supportando le decisioni relative ai parametri di coltivazione e alle applicazioni di bioraffinazione. In questo caso, per stress si intende la mancanza di nutrienti chiave per la crescita, come il fosforo o l’azoto. “Quando l’organismo avverte la mancanza di questi nutrienti, inizia ad accumulare lipidi per sopravvivere. Abbiamo usato questa capacità come strategia per creare un accumulo del metabolita di interesse. In altre parole, abbiamo stressato l’organismo eliminando i nutrienti necessari alla crescita. Allo stesso tempo, poiché l’organismo cresceva più lentamente, la proporzione di altri metaboliti, come proteine e carboidrati, diminuiva. È importante identificare il composto di interesse e assicurarsi di raggiungere il giusto equilibrio per lo studio“, ha detto Ríos. Lo stress ha aumentato la produzione di lipidi e idrocarburi rispettivamente del 49% e del 29%, ma le proteine sono diminuite dal 32% della composizione totale al 26%. Le proporzioni di carboidrati (15% del totale) e pigmenti (0,41%-0,86%) erano simili nella crescita stressata e non stressata.
